15일 허가·심사 규정 개정고시…22일 민원설명회 개최
식품의약품안전청이 국내 업체의 바이오시밀러 제품 개발을 적극 지원하고 나선다.
식약청은 15일 '동등생물의약품(바이오시밀러) 허가·심사를 위한 규정'을 개정 고시한 데 이어 22일 오후 3시 한국과학기술회관 중회의실에서 민원설명회를 연다.
식약청에 따르면 지금까지 바이오시밀러 허가제도를 도입한 나라는 유럽(EU) 뿐으로, 한국이 세계에서 두 번째 나라가 됐다.
새로운 허가심사 규정에는 바이오시밀러에 대한 정의가 신설됐으며, 허가를 받기 위한 자료제출 범위가 명시됐다. 식약청은 또 올해 4월 조직안에 '바이오의약품정책과'와 '첨단바이오제품과'를 신설하기도 했다.
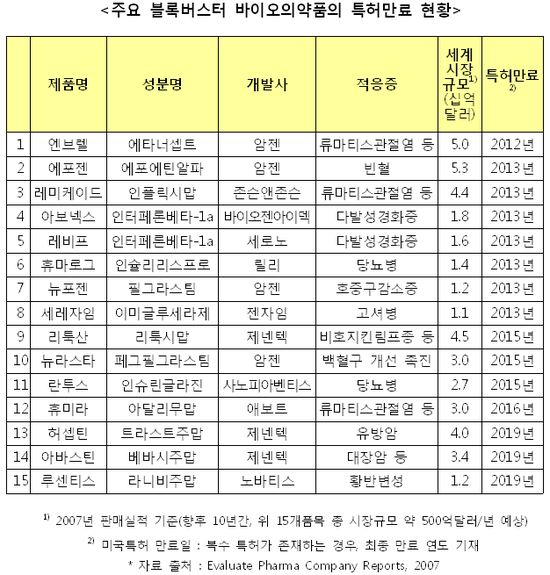
식약청은 "세계 의약품 시장에서 생물의약품 점유율이 크게 신장될 것으로 전망되고 있으며(2012년 전체 시장의 1/4 규모), 인슐린을 시작으로 생물의약품의 특허기간이 대거 만료될 예정"이라며 "바이오시밀러 의약품의 세계 시장 선점을 통해 신성장동력산업으로 성장할 수 있도록 지원할 방침"이라고 말했다.
한편 최근 삼성전자를 비롯 국내 대기업들이 바이오시밀러 분야 진출을 선언하는 등 연구개발에 대한 투자를 늘리고 있는 추세다.
저작권자 © 의협신문 무단전재 및 재배포 금지


